第二例艾滋病患者被治愈!但疗法没什么突破,靠的全是好运气
近日,“世界上第二例艾滋病患者被证明治愈”的病例报告发表在了医学杂志《柳叶刀》子刊《柳叶刀·艾滋病病毒》(Lancet HIV)上[1]。
来源:Lancet HIV
在2019年3月,这位病人被“治愈”的消息一度刷屏。但当时研究团队指出,仍然会继续监测他的情况,说“艾滋病治愈”还为时过早。
而2020年3月的新研究,为我们带来了他“已经被证明治愈”的后续报道。
那么,这对于广大艾滋病患者而言,是不是一个重磅的好消息呢?人类离战胜艾滋病已经很近了吗?
先别激动,让我们来看看他的治疗过程到底是怎么回事。
“伦敦病人”的治疗经历
这位艾滋病患者来自英国伦敦,代号“伦敦病人”,早在2003年他查出感染了艾滋病病毒,2012年开始接受抗逆转录病毒治疗。后来,他又不幸得了晚期霍奇金淋巴瘤。
做了化疗之后,他又在2016年接受了干细胞移植,随后又接受了16个月的抗逆转录病毒治疗。
到了2019年3月,他已接受干细胞移植治疗3年、抗逆转录病毒药已经停药1年半,血液中一直没有检测出艾滋病毒载量。
到了2020年3月,他在停止抗逆转录病毒治疗30个月后,血液、脑脊液、肠组织和淋巴组织中都没有检测到具有复制能力的HIV病毒。
此外,他的免疫细胞99%都来自供体的干细胞,这说明干细胞移植已成功。
研究团队认为,这一切发现都证明他是长期缓解(治愈)了。当然,研究人员也表示,这位病人仍然需要长期监测,看HIV病毒会不会在他体内反弹、重现。
而最近,这位神秘的伦敦病人走出阴霾后,经再三考虑,决定公开自己的身份——
他的真名叫亚当·卡斯蒂列霍(Adam Castillejo),40岁,住在伦敦东区[2]。

亚当·卡斯蒂列霍(Adam Castillejo)
来源:纽约时报
虽然现在的他看上去健康、快乐,但他坦言,在过去近10年的痛苦治疗中也曾绝望过。
但正因为如此,他想用自己的故事给大家带去乐观和鼓励。“我想成为希望的大使。”
“伦敦病人”,和同病相怜的“柏林病人”
不过,这个“伦敦病人”,和多年前“柏林病人”的故事并没有本质区别。都是一个非常偶然的事件。
有多偶然呢?
要同时凑齐三大条件:艾滋病人、霍奇金淋巴瘤、做干细胞移植时刚好碰上CCR5基因突变的供体。
这种概率,目前全世界也才两例,比买彩票难多了。
在很多人眼里,艾滋病遭遇癌症晚期,人类最怕的两个大病都凑齐了,可以说是雪上加霜。
但其实,艾滋病人得淋巴瘤的情况并不罕见。
由于体内的免疫细胞被病毒破坏,艾滋病人的免疫力长期低下,出现各种机会性感染和肿瘤的几率大大增加,这其中就有艾滋病相关的淋巴瘤。
而干细胞移植,是治疗淋巴瘤和白血病的有效方法之一。
干细胞移植的目的是在放化疗结束后,用健康的造血干细胞取代病人原有的病态干细胞,让它们重新产生新的血细胞。
有时,这些新生血细胞还有额外的作用,能把放化疗后的癌细胞的“残余势力”也统统消灭。
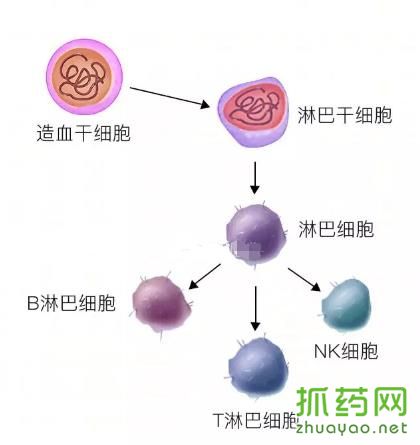
造血干细胞的分化
大家注意,就是这里的“干细胞移植”,成了这位哥儿们的救命稻草。
当时,由于他的父亲是西班牙和荷兰混血裔,他跟好几个捐赠者都匹配。
关键是他的运气好到爆棚:其中一位德国捐赠者带有一种罕见的基因突变——CCR5-delta 32突变!
带有这种突变的人,对艾滋病几乎“天然免疫”——
因为HIV病毒要想进入T细胞搞破坏,主要靠的就是CCR5蛋白这个“锁眼”。
但存在CCR5突变的人,他们的CD4+ T细胞完全不表达CCR5蛋白!
头回碰到这种操作,艾滋病毒也傻眼了,没有“锁眼”还怎么开门?
进入不了T细胞,没法复制繁衍,艾滋病毒就只能慢慢死掉了。
早在2007年,世界上第一例艾滋病治愈者——“柏林病人”(Timothy Brown),就是这样被治愈的。当时他患上了白血病,做骨髓移植的时候,移植者的骨髓刚好就带有这种突变基因。后来,艾滋病毒就从他体内消失了。
正因为这样,“柏林病人”成为公认的世界首位得到功能性治愈的艾滋病患者。
时隔13年后的今天,“伦敦病人”跟他的情况非常相似。
很多人肯定会问:这种情况能复制吗?是不是找CCR5基因突变的人做骨髓移植,就能治愈艾滋病了?
没那么简单。
为何“艾滋病治愈”难以复制?
自从“柏林病人”出现后,科学家们又在至少2名患有淋巴瘤的HIV感染者身上尝试过这种方法,但并没有找到携带CCR5突变的供体,只是单纯进行了骨髓移植。
当时他们的猜想是,就算没有CCR5突变基因,“移植物抗宿主病”或许也能杀死HIV病毒——移植后的骨髓细胞有可能产生新的免疫细胞,去攻击原始细胞。
2014年,著名的被功能性治愈的“密西西比婴儿”体内重新出现了HIV病毒。后来,第二例被“治愈”的艾滋病婴儿也重新出现了HIV感染迹象。
一开始,他们体内似乎没有HIV病毒了,但几个月后病毒又会“卷土重来”,只好重新服用抗逆转录病毒药物。
这再次证明,骨髓供体携带的CCR5基因突变才是关键。
为什么不能找到一个带有CCR5突变的捐赠者来试试看呢?
这就涉及到配型的问题。因为捐赠者的干细胞不但需要和患者配型成功,还要携带罕见的CCR5纯合基因突变。
如此小的概率下,要想找到合适的捐献者难度极大,所以这个方法很难在人群中推广。
另外一方面,干细胞移植也不是随便用的,有很大风险。只有患上特定疾病(比如白血病、淋巴瘤等)需要干细胞移植,才能用这种方法,而不是随便找一个HIV感染者就能做试验。
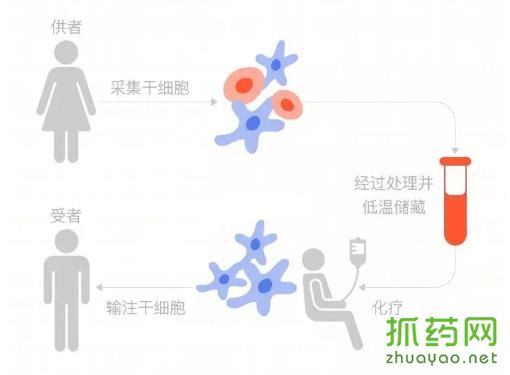
干细胞移植过程
或许更有可能的途径是,通过基因编辑手段,把病人的外周血CD4+T细胞和造血干细胞CCR5基因全部敲除,再回输到病人体内。这个方法目前还在探索当中。
最后一个问题就是,艾滋病病毒也在找其他出路,没有在“一棵树上吊死”。
某些型别的HIV病毒并不依赖于CCR5,它们还找到了其他“锁眼”,如CXCR4、CCR2b和 CCR3等,一样可以进入细胞。
2018年年底震惊全球的“艾滋病免疫基因编辑婴儿”就存在这样的漏洞——即使敲掉了CCR5基因,婴儿仍然可能被其他型别的HIV病毒感染[3-4]。
总之,这种疗法风险很大,费用也非常昂贵,难以复制,无法效仿。
如今,艾滋病人只要坚持每天服药,绝大多数都能长期生存。
所以对于这种疗法,我们可以抱有期待,但要真正应用到广大艾滋病患者身上,还有相当长的一段距离。
希望在人类战胜艾滋病的道路上,能听到更多好消息。
参考文献
[1]https://www.thelancet.com/journals/lanhiv/article/PIIS2352-3018(20)30069-2/fulltext
[2]https://www.nytimes.com/2020/03/09/health/hiv-aids-london-patient-castillejo.html
[3]曾毅. 警惕艾滋病(修订版)[M]. 清华大学出版社, 2010.
[4] Brelot A, Chakrabarti L A. CCR5 revisited: how mechanisms of HIV entry govern AIDS pathogenesis[J]. Journal of molecular biology, 2018.

